Szczepionka przeciw kleszczowemu zapaleniu mózgu
Podsumowanie
O chorobie
Co to jest kleszczowe zapalenie mózgu?
Jakie są objawy kleszczowego zapalenia mózgu?
Jak poważne mogą być objawy kleszczowego zapalenia mózgu?
Jak często kleszczowe zapalenie mózgu występuje w Polsce?
Gdzie są obszary endemicznego wykrywania KZM w Polsce?
Gdzie i jak często kleszczowe zapalenie mózgu występuje na świecie?
O szczepionce
Jakie rodzaje szczepionek przeciw kleszczowemu zapaleniu mózgu są dostępne w Polsce?
Dlaczego warto się szczepić przeciw kleszczowemu zapaleniu mózgu?
Kto i kiedy powinien zostać zaszczepiony przeciw kleszczowemu zapaleniu mózgu?
Kto nie powinien zostać zaszczepiony przeciw kleszczowemu zapaleniu mózgu?
Jakie ryzyko jest związane ze szczepieniem przeciw kleszczowemu zapaleniu mózgu?
Jaka jest skuteczność szczepionek przeciw kleszczowemu zapaleniu mózgu?
Jakie szczepionki przeciw kleszczowemu zapaleniu mózgu są dostępne w Polsce?
Kalendarz szczepień
Szczepionka przeciwko kleszczowemu zapaleniu mózgu w Programie Szczepień Ochronnych
Czytaj więcej
Jakie są drogi zakażenia wirusem kleszczowego zapalenia mózgu?
Jak często należy podawać dawki przypominające szczepionki przeciw kleszczowemu zapaleniu mózgu?
Czy dwie dostępne szczepionki przeciw kleszczowemu zapaleniu mózgu można stosować wymiennie?
Kiedy najlepiej zaszczepić się przeciw kleszczowemu zapaleniu mózgu aby być odpornym w czasie letnich wakacji?
Czy można sprawdzić, że kleszcz który nas ugryzł był zakażony wirusem kleszczowego zapalenia mózgu?
Czy można się zaszczepić przeciw kleszczowemu zapaleniu mózgu po ukąszeniu przez zarażonego kleszcza?
Czy można zaszczepić się na kleszcze?
Czy można zaszczepić się przeciw boreliozie?
Podsumowanie
O chorobie
Kleszczowe zapalenie mózgu to ostra choroba wirusowa, która często wiąże się z powikłaniami neurologicznymi. Źródłem infekcji może być ukąszenie przez zakażonego kleszcza, poprzez spożycie niepasteryzowanego mleka zakażonego zwierzęcia lub znacznie rzadziej poprzez transfuzję krwi lub przeszczep narządu od osoby w fazie wiremii. Okres inkubacji choroby wynosi od 7 do 14 dni. W pierwszej fazie, zakażenie przebiega bezobjawowo lub wywołuje objawy podobne do grypy. U części osób zakażonych, po 7-14 dniach dochodzi do zajęcia ośrodkowego układu nerwowego. Może dojść do zapalenia rdzenia kręgowego, zapalenia opon mózgowo-rdzeniowych lub zapalenie mózgu i opon mózgowo-rdzeniowych. U 35%–58% chorych z zajęciem ośrodkowego układu nerwowego dochodzi do trwałych powikłań neurologicznych, a u ok. 1/100 chorych zakażenie kończy się zgonem.
Pamiętaj, że:
- Nie da się łatwo uchronić przed ukąszeniami kleszczy i nie da się przewidzieć czy dany kleszcz przenosi wirusa,
- Szczepienie jest obecnie jedynym skutecznym sposobem uchronienia się przed tą ciężką chorobą i jej powikłaniami,
- Żeby utrzymać ochronę przed zakażeniem konieczne jest przyjęcie 3 dawek szczepienia pierwotnego oraz dawkę przypominającą co 3-5 lat.
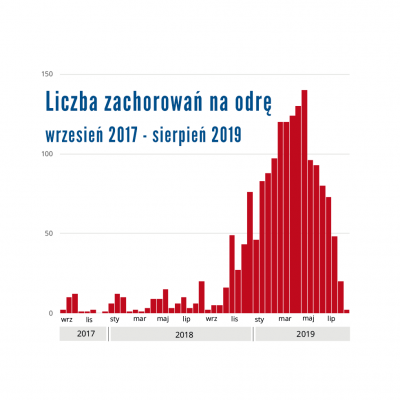
W Polsce liczbę zachorowań na kleszczowe zapalenie mózgu szacuje się na 150 do ponad 250 przypadków rocznie. Najwięcej zachorowań obserwuje się w rejonach północno-wschodniej Polski (do 80% zakażeń w danym roku). Sezonowość zachorowań wiąże się z dwoma okresami aktywności kleszczy: dominującym – wiosenno-letnim i słabszym – jesiennym. Na świecie odnotowuje się rocznie ponad 10,000 zachorowań na kleszczowe zapalenie mózgu, głównie w północno-wschodnich oraz środkowych regionach Europy oraz w północnych regionach Azji.
O szczepionce
Dostępne są inaktywowane szczepionki przeciw kleszczowemu zapaleniu mózgu. Aby skutecznie ochronić się przed zakażeniem konieczne jest przyjęcie 3 dawek szczepienia pierwotnego oraz dawek przypominających co 3-5 lat. Zaszczepienie zimą lub wczesną wiosną zapewnia ochronę już od początku aktywności kleszczy (od kwietnia do października). Szczepionki zalecane są w określonych grupach zawodowych oraz osobom przebywającym na obszarach endemicznych. Szczepionki przeciw kleszczowemu zapaleniu mózgu cechuje wysoka skuteczność – na 100 szczepionych powyżej 95 osób wytwarza przeciwciała ochronne zabezpieczające przed powikłaniami.
Przeciwwskazaniem do szczepienia przeciwko kleszczowemu zapaleniu mózgu są reakcja anafilaktyczna po wcześniejszej dawce szczepionki, ostra choroba przebiegająca z gorączką oraz nasilona reakcja alergiczna na substancje pomocnicze wchodzące w skład szczepionki. Po podaniu szczepionki mogą występować miejscowe niepożądane odczyny poszczepienne, głównie przemijający ból w miejscu wstrzyknięcia obrzęk, bolesność, zaczerwienienie. Może też rzadko dochodzić do odczynów uogólnionych, np. przejściowy stan gorączkowy, ogólne osłabienie, objawy grypopodobne.
- Balogh Z, Ferenczi E, Szeles K, Stefanoff P, Gut W, Szomor KN, Takacs M, Berencsi G.Tick-borne encephalitis outbreak in Hungary due to consumption of raw goat milk. J Virol Methods. 2010 Feb;163(2):481-5.
- Barret N. P, Plotkin S.A., Ehrlich H.J.: Tick-borne encephalitis virus vaccines. W: Plotkin S., Orenstein W., Offit P. (red.): Vaccines, 7th edition, Elsevier, 2017.
- Siennicka J, Trzcińska A, Gut W. Immunity against tick borne encephalitis virus (TBE) in population of forest workers in Bialowieza. Przegl Epidemiol. 2010;64(2):303-5.
- Stefanoff P, Rosinska M, Samuels S, White DJ, Morse DL, Randolph SE. A national case-control study identifieshuman socio-economic status and activities as risk factors for tick-borne encephalitis in Poland. PLoS One. 2012;7,9.
- Stefanoff P, Zielicka-Hardy A, Hlebowicz M, Konior R, Lipowski D, Szenborn L, Siennicka J, Orlikova H, Working Group TE. New endemic foci of tick-borne encephalitis (TBE) identified in districts where testing for TBE was not available before 2009 in Poland. Parasit Vectors. 2013 Jun 18;6:180.
- http://www.tbe-info.com/tbe.aspx_param_target_is_150790_and_l_is_2.v.aspx
- Choroby zakaźne i zatrucia w Polsce, NIZP-PZH
- Lipowski D. i wsp. A Cluster of Fatal Tick-borne Encephalitis Virus Infection in Organ Transplant Setting. J Infect Dis. 2017 Mar 15;215(6):896-901.
- Tick-borne encephalitis: a review of epidemiology, clinical characteristics, and management
Petra Bogovic, Franc Strle. World Journal of Clinical Cases, 2015; 3 (5): 430–441 - Stryczyńska-Kazubska J., Małecka I., Wysocki J. Szczepienia dzieci z chorobami alergicznymi. Standardy Medyczne/Pediatria 2016, 13, 61-65.
- Barrett PN, Portsmouth D. A novel multivalent OspA vaccine against Lyme borreliosis shows promise in Phase I/II studies. Expert Rev Vaccines. 2013 Sep;12(9):973-5.
- Poland GA. Vaccines against Lyme disease: What happened and what lessons can we learn? Clin Infect Dis. 2011 Feb;52 Suppl 3:s253-8.
- P. Stefanoff, B. Rubikowska, J. Bratkowski, Z. Ustrnul, S.O. Vanwambeke, M. Rosinska. A predictive model identified tick-borne encephalitis high risk areas in regions where no cases were reported previously, Poland, 1999-2012. International Journal of Environmental Research and Public Health 2018; 15(4), 677.
- P. Stefanoff, A. Zielicka-Hardy, M. Hlebowicz, R. Konior, D. Lipowski, L. Szenborn, J. Siennicka, H. Orlikova. TBE enhanced surveillance working group (2013): New endemic foci of tick-borne encephalitis identified in districts where testing for TBE was not available before, Poland, 2009. Parasites & Vectors 2013; 6(1): 180.
- P. Stefanoff, M. Pfeffer, W. Hellenbrand, J. Rogalska, F. Rühe, A. Makówka, J. Michalik, B. Wodecka, A. Rymaszewska, D. Kiewra, A. Baumann-Popczyk, G. Dobler. Virus detection in questing ticks is not a sensitive indicator for risk assessment of tick-borne encephalitis in humans. Zoonoses and Public Health 2012; 60(3): 215-226.
- P. Stefanoff, J. Siennicka, J. Kaba, M. Nowicki, E. Ferenczi, W. Gut. Identification of new endemic tick-borne encephalitis foci in Poland – a pilot seroprevalence study in selected regions. International Journal of Medical Microbiology 2008; 298 (Suppl. 1): 102-107.
- Broker M. i wsp. Aret ich-borne encephalitis vaccines interchangeable? Expert Rev. Vaccines, 2006, 5(4), 461-466.
- Kollaritsch H i wsp. Background document on vaccines and vaccination against tick-borne encephalitis. Geneva, WHO Startegic Advisory Group of Experts on Immunisation, 2011.
- Vaccines against tick-borne encephalitis: WHO position paper. Weekly epidemiological record 2011, 86, 24, 241-256.
- Heinz F.X., Holzmann H., Essl A. i wsp.: Field effectiveness of vaccination against tick-borne encephalitis. Vaccine, 2007; 25: 7559–7567.